咨詢熱線(xiàn)
400-810-0881
新(xīn)品推薦 | CAR-T靶向的熒光素酶報告細胞系
研究背景
嵌合抗原受體(tǐ)(CAR)-T細胞在治療惡性腫瘤,特别是非實體(tǐ)瘤方面表現出顯著的療效。
CAR-T細胞已被證明是一種新(xīn)型的“活體(tǐ)”療法,它利用(yòng)病人的免疫系統來識别特定的腫瘤相關抗原,并将工(gōng)程化的T細胞重新(xīn)定向到更有(yǒu)針對性的腫瘤細胞。
體(tǐ)外評估CAR-T細胞的生物(wù)功能(néng)通常涉及一系列勞動密集型的共培養實驗和免疫測定,并且在驗證新(xīn)的CAR-T細胞的過程中(zhōng),重複性常常受到供體(tǐ)之間的差異和其他(tā)影響而不穩定。
為(wèi)了解決這一挑戰,研究學(xué)者們提出了CAR-T靶向的熒光素酶報告癌症細胞,這些細胞具(jù)有(yǒu)CD19、CD20和HER2的高内源表達,并且表現出敏感和穩定的熒光素酶表達報告,使您能(néng)夠實時監測候選CAR-T效應細胞在細胞毒性和細胞活力測定中(zhōng)的效力和功效,從而實現免疫治療突破。
解決思路
基于CAR-T細胞的療法已成為(wèi)治療特定白血病、淋巴瘤和骨髓瘤的一種有(yǒu)前景的免疫療法。
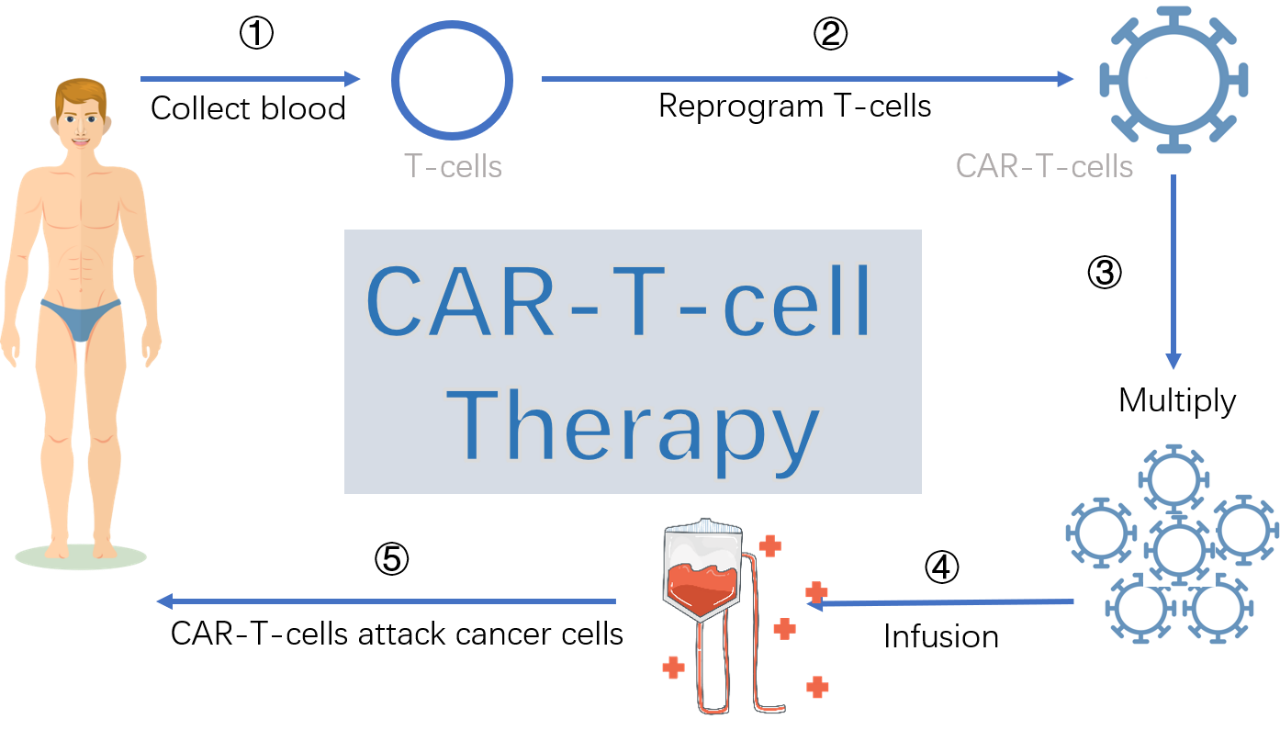
在這種治療難治性癌症的令人興奮的方法中(zhōng),通過單采從患者血液中(zhōng)分(fēn)離T細胞,然後将這些細胞與細胞因子白介素2和抗CD3抗體(tǐ)一起孵化以刺激增殖。将參與移植物(wù)排斥反應的基因進行離體(tǐ)沉默,改善了輸注後T細胞的穩定性。一旦擴增,适當的CAR通過逆轉錄病毒轉導被引入細胞中(zhōng)。然後這些有(yǒu)效的CAR-T細胞被輸回病人體(tǐ)内,使其對腫瘤細胞發揮細胞毒性作(zuò)用(yòng)1。
目前在開發新(xīn)的CAR結構方面已經投入了大量的研究工(gōng)作(zuò),以增加目标癌症類型的範圍并提高其抗腫瘤的療效。CAR-T發展過程中(zhōng)的一個瓶頸是評估CAR-T細胞的生物(wù)功能(néng)。以往的經驗中(zhōng),會使用(yòng)放射性⁵¹Cr釋放測定法,但是該方法隻能(néng)在單一時間點獲得數據,且具(jù)有(yǒu)内在的放射性,試劑的半衰期、保護措施和廢物(wù)處理(lǐ)都是關鍵因素。
研究CAR-T效應功能(néng)的一種方法是生物(wù)發光(BLI)報告試驗,這種方法消除了⁵¹Cr釋放和染料負載測定的擔憂。在BLI報告基因測定中(zhōng),将構成性表達熒光素酶的靶細胞與候選效應細胞共同培養,并通過BLI信号的損失來監測細胞
毒性4。除了易于使用(yòng)外,BLI試驗中(zhōng)表達熒光素酶的靶細胞可(kě)以提高實驗間的可(kě)重複性。
為(wèi)了生成CAR-T靶向熒光素酶報告細胞,研究者們将Lenti-LUC2熒光素酶報告劑引入親代細胞系,進行抗生素選擇和單細胞分(fēn)選,分(fēn)離出具(jù)有(yǒu)高熒光素酶表達的穩定克隆。
然後通過比較低通量和高通量報告細胞,驗證目标抗原和熒光素酶的表達穩定性。一旦選擇了穩定的克隆并驗證了抗原和熒光素酶的表達,報告細胞系就會用(yòng)嘗試過的鑒定方法,如短串聯重複(STR)分(fēn)析、支原體(tǐ)檢測以及細胞生長(cháng)速度和形态學(xué)檢測,對其進行特征分(fēn)析和鑒定。
CAR-T靶向熒光素酶報告細胞的性能(néng)在T細胞共培養實驗中(zhōng)得到了驗證。研究者們采用(yòng)了市售的針對CD19、CD20和HER2的CAR-T細胞,将來自同一供體(tǐ)的空載體(tǐ)轉導的T細胞與之配對作(zuò)為(wèi)對照。CAR-T細胞對目标腫瘤細胞的細胞毒性是用(yòng)熒光素酶測定法、市售的效力測定法以及明場和熒光活細胞成像測定法來測量的。
研究者們的結果表明,熒光素酶報告系統是測量癌症和T細胞體(tǐ)外共培養物(wù)中(zhōng)生物(wù)過程的一種簡單、強大和高度敏感的手段。
總之,來自ATCC的CAR-T靶向熒光素酶報告細胞是研究CAR-T生物(wù)功能(néng)和驗證用(yòng)于癌症免疫治療的新(xīn)CAR-T藥物(wù)的特征鮮明、重複性高的工(gōng)具(jù)。
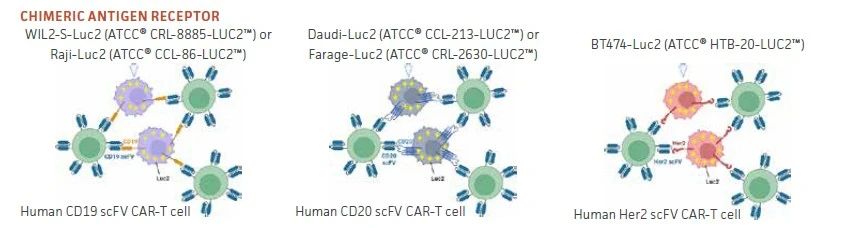
圖1:CAR-T靶向熒光素酶報告細胞。示意圖顯示表達CD19+WIL2-S-Luc2和Raji-Luc2、CD20+Daudi-Luc2和Farage-Luc2以及HER2+BT-474-Luc2的CAR-T靶細胞分(fēn)别被CD19、CD20和HER2靶向的CAR-T細胞包圍并攻擊。
新(xīn)産(chǎn)品的誕生
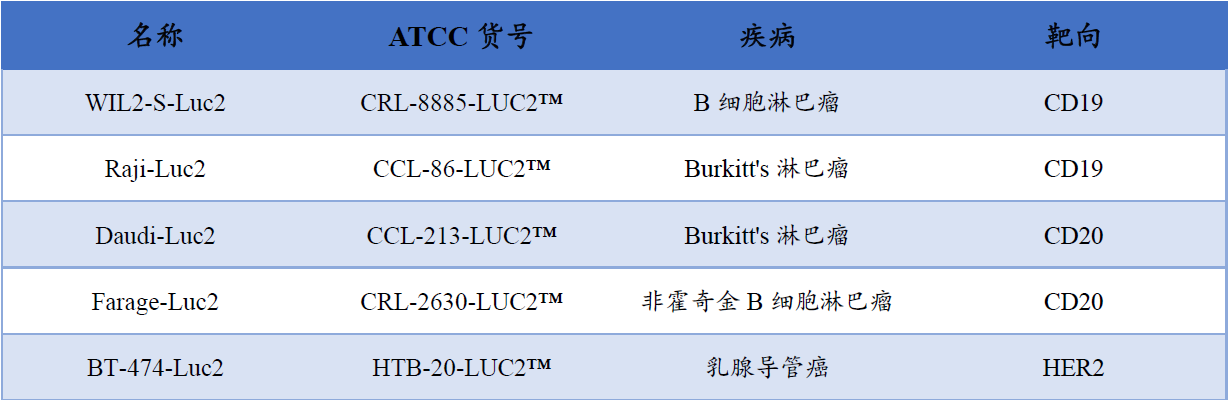
目前,ATCCT推出的CAR-T靶向熒光素酶報告細胞産(chǎn)品如下:
這些方便的報告标記細胞可(kě)以消除涉及放射性或熒光染料标記的工(gōng)作(zuò)流程,使細胞保持靶抗原和熒光素酶的高表達,最高可(kě)達到30個群體(tǐ)倍增。這些靈活的靶細胞也可(kě)以被納入其他(tā)免疫腫瘤學(xué)應用(yòng)中(zhōng),如ADCC和自然殺傷(NK)細胞的細胞毒性試驗。
靶抗原和熒光素酶的高表達穩定性
高信噪比(S/N)
生理(lǐ)相關的低E:T比率
高效能(néng)、完全認證的細胞系
易于使用(yòng)的報告系統
可(kě)進行實時活細胞成像
主要實驗數據
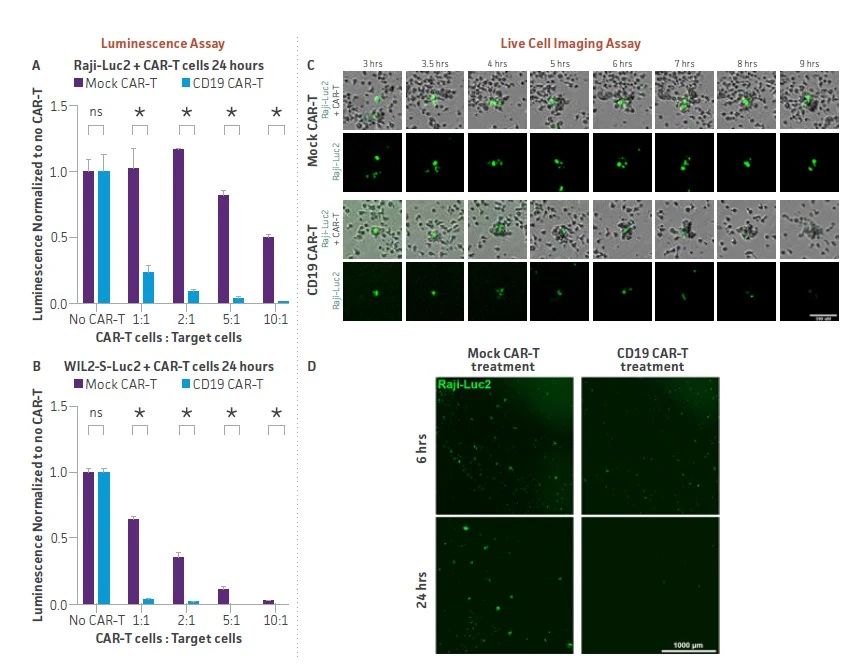
圖 2:CAR-T靶向熒光素酶報告細胞可(kě)被納入多(duō)種CAR-T療效檢測中(zhōng)。(A)表達CD19的Raji-Luc2細胞(B)WIL2-S-Luc2細胞作(zuò)為(wèi)CD19 CAR-T或Mock CAR-T(對照)效應細胞的靶細胞,來自同一供體(tǐ)的效應細胞與靶細胞的比例為(wèi)所示。加入熒光素酶檢測底物(wù),并檢測發光信号。信号消失表示細胞死亡;通過CD19靶向的CAR-T細胞的劑量依賴性特異性殺傷大于用(yòng)模拟CAR-T細胞觀察到的非特異性殺傷。此外,用(yòng)細胞标記染料對Raji-Luc2細胞染色,然後在與CD19 CAR-T效應細胞共培養期間進行實時熒光成像測量。(C)Raji-Luc2細胞(綠色)被效應T細胞包圍,與Mock-CAR-T細胞共培養相比,導緻熒光下降。(D)在CD19 CAR-T效應細胞共培養6小(xiǎo)時和24小(xiǎo)時後,研究學(xué)者們觀察到熒光細胞的數量減少;然而,在與Mock CAR-T細胞共培養時,有(yǒu)許多(duō)Raji-LUC2細胞存在。這些結果表明,ATCC CAR-T靶向熒光素酶報告細胞可(kě)用(yòng)于實時評估CAR-T細胞在生物(wù)發光實驗和活細胞實時成像中(zhōng)的潛力。
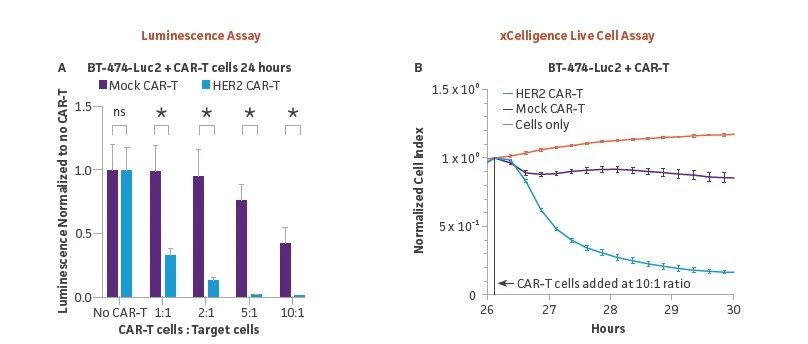
圖3:HER2 CAR-T對BT-474-Luc2的體(tǐ)外殺傷力檢測,使用(yòng)發光法和xCelligence測量。(A) 将HER2陽性的BT-474-Luc2細胞(5 x 103)接種到96孔闆中(zhōng),作(zuò)為(wèi)同一供體(tǐ)的HER2 CAR-T或Mock CAR-T(對照)的靶細胞,CAR-T細胞與靶BT-474-Luc2細胞分(fēn)别以不同的比例(1:1,2:1,5:1,10:1)接種。在共培養24小(xiǎo)時後,将Bright-Glo加入到指定的孔中(zhōng)。使用(yòng)發光闆閱讀器在10分(fēn)鍾内讀取闆的發光情況,确定HER2 CAR-T細胞具(jù)有(yǒu)劑量依賴性的特異性殺傷力,大于用(yòng)模拟CAR-T細胞觀察到的非特異性殺傷力(*=差異明顯,ns=差異不明顯,使用(yòng)非配對t檢驗,單一的集合方差)。(B)HER2 CAR-T細胞以10:1的比例針對2×10⁴HER2陽性的BT-474-Luc2,用(yòng)xCELLigence系統測量細胞殺傷力。來自同一供體(tǐ)的模拟CAR-T細胞被用(yòng)作(zuò)對照。
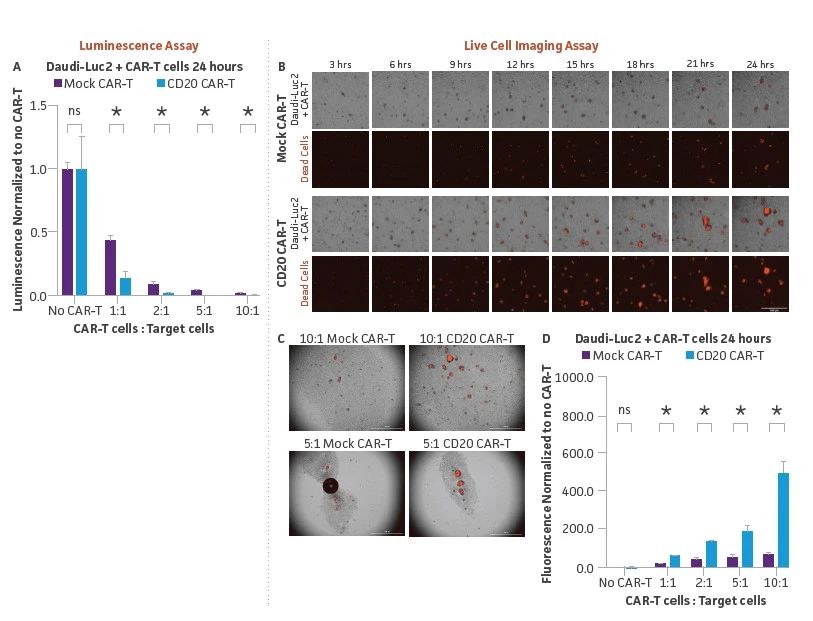
圖4:使用(yòng)發光和活細胞成像技(jì )術對Daudi-Luc2進行CD20 CAR-T體(tǐ)外殺傷試驗。(A) 将CD20陽性的Daudi-Luc2細胞(5 x 103)接種到96孔闆中(zhōng),并用(yòng)來自同一供體(tǐ)的CD20 CAR-T或Mock CAR-T(對照)的靶細胞,CAR-T細胞與靶Daudi-Luc2細胞分(fēn)别以不同比例(1:1,2:1,5:1,10:1)接種。在共培養24小(xiǎo)時後,在指定的孔中(zhōng)加入Bright-Glo。用(yòng)發光闆閱讀器在10分(fēn)鍾内讀取闆的發光,确定與CD20 CAR-T細胞有(yǒu)劑量依賴性的特異性殺傷,這比用(yòng)模拟CAR-T細胞觀察到的非特異性殺傷要大(*=差異明顯,ns=不明顯,使用(yòng)非配對t檢驗,有(yǒu)一個集合的方差)。(B) 在培養基中(zhōng)存在Incucyte Cytotox紅色染料的情況下,将Daudi-Luc2細胞(5 x 103)與CD20 CAR-T細胞或Mock CAR-T細胞共同培養,并在24小(xiǎo)時内每小(xiǎo)時測量一次實時熒光成像,結果與CD20 CAR-T共同培養時,熒光強度比與Mock-CAR-T細胞共同培養時增加。(C)與CD20 CAR-T細胞共培養24小(xiǎo)時後,與Mock CAR-T細胞共培養相比,Daudi-Luc2顯示死亡(紅色)熒光細胞數量增加。(D) 對聚集的紅色熒光進行了量化和比較(*=差異明顯,ns=差異不明顯,使用(yòng)非配對t檢驗,具(jù)有(yǒu)單一合并方差)。
結 論
CAR-T靶向熒光素酶報告細胞在測量靶細胞殺傷方面具(jù)有(yǒu)優勢,無需使用(yòng)放射性⁵¹Cr釋放試驗或預先标記細胞進行CAR-T功能(néng)評估4。
此外,利用(yòng)細胞形态學(xué)、生長(cháng)動力學(xué)和STR分(fēn)析對這些報告細胞系進行了表征和鑒定7。通過比較低通量和高通量報告細胞,驗證了目标抗原和熒光素酶的表達穩定性。
重要的是,這些熒光素表達細胞的細胞毒性可(kě)以通過實時的BLI信号損失來測量,這種損失通過活細胞成像和細胞毒性染料吸收試驗得到證實。綜上所述,特征明确的熒光素酶報告細胞系能(néng)夠實現方便和一緻的信号量化,并且它們是研究CAR-T生物(wù)功能(néng)和驗證用(yòng)于癌症免疫治療的新(xīn)CAR-T藥劑的易用(yòng)工(gōng)具(jù)。這些強大的細胞模型代表了腫瘤學(xué)研究中(zhōng)最主要的患者來源的癌和淋巴瘤癌系。
CAR-T靶向熒光素酶報告細胞是從ATCC廣泛的已建立的癌症細胞系目錄中(zhōng)挑選出來的,這些細胞系含有(yǒu)一些最普遍的癌症抗原的高内源性表達,這使得它們成為(wèi)開發更合适的CAR-T細胞療法的更具(jù)生理(lǐ)相關性的體(tǐ)外工(gōng)具(jù)。
參考文(wén)獻:
1. Kiesgen S, et al. Comparative analysis of assays to measure CAR T-cell-mediated cytotoxicity. Nat Protoc 16: 1331-1342, 2021. PubMed: 33589826
2. Jackson HJ, et al. Driving CAR T-cells forward. Nat Rev Clin Oncol 13: 370-383, 2016. PubMed: 27000958
3. Sterner RC, Sterner RM. CAR-T cell therapy: current limitations and potential strategies. Blood Cancer J 11: 69, 2021. PubMed: 33824268
4. Riss T, et al. Cytotoxicity Assays: In Vitro Methods to Measure Dead Cells, in Assay Guidance Manual. (eds. S. Markossian et al.) (Bethesda (MD); 2004). PubMed: 31070879
5. Meijer TWH, et al. Targeting glucose and glutamine metabolism combined with radiation therapy in non-small cell lung cancer. Lung Cancer 126: 32-40, 2018. PubMed: 30527190
6. Lisby AN, et al. Evaluation of CAR-T cell cytotoxicity: Real-time impedance-based analysis. Methods Cell Biol 167: 81-98, 2022. PubMed: 35153000
7. Capes-Davis A, et al. Check your cultures! A list of cross-contaminated or misidentified cell lines. Int J Cancer 127: 1-8 2010. PubMed: 20143388
 京公(gōng)網安(ān)備11010502040370号 技(jì )術支持:青雲軟件
京公(gōng)網安(ān)備11010502040370号 技(jì )術支持:青雲軟件