AAV——用(yòng)于哺乳動物(wù)基因表達的通用(yòng)病毒工(gōng)具(jù)
腺相關病毒(AAV)已成為(wèi)科(kē)學(xué)研究和臨床應用(yòng)中(zhōng)最受歡迎的病毒工(gōng)具(jù)。AAV可(kě)用(yòng)于在多(duō)種細胞中(zhōng)瞬時表達目的基因。大約50年前,它首次被描述為(wèi)腺病毒制劑的污染物(wù),因此得名(míng)腺相關病毒(Atchison et al., 1965)。AAV屬于細小(xiǎo)病毒科(kē)的單鏈DNA病毒。它是由包裝(zhuāng)在二十面體(tǐ)衣殼中(zhōng)的“簡單”基因組構成。它沒有(yǒu)脂質(zhì)外殼,也稱為(wèi)包膜,因此不能(néng)支持向其表面添加糖蛋白,如VSV-G。在研究應用(yòng)中(zhōng),通常将基因組去除,以便為(wèi)基因傳遞提供寶貴的空間并增加安(ān)全性。通過提供編碼複制功能(néng)的酶和衣殼蛋白的基因,您可(kě)以在組織培養環境中(zhōng)輕松構建病毒。這使研究人員能(néng)夠在受控環境中(zhōng)産(chǎn)生更多(duō)病毒。盡管AAV可(kě)從多(duō)種生物(wù)中(zhōng)分(fēn)離出來的,但它與疾病無關,它被認為(wèi)是生物(wù)安(ān)全1級(BSL1)病毒。
重組AAV (rAAV)工(gōng)具(jù)的優化設計
AAV可(kě)用(yòng)于多(duō)種應用(yòng),包括特定細胞類型中(zhōng)的瞬時基因表達,CRISPR基因組編輯,光遺傳學(xué)和化學(xué)遺傳學(xué)實驗。如果您不熟悉使用(yòng)rAAV作(zuò)為(wèi)基因傳遞工(gōng)具(jù),那麽在開始實驗之前您應該考慮以下事項:
1、基因載量:即使除去基因組的rAAV也隻具(jù)有(yǒu)~4.7 kb的基因載量,這是該病毒用(yòng)于基因載體(tǐ)的關鍵限制之一。然而,如果您感興趣的基因足夠小(xiǎo),您可(kě)以設計單個rAAV載體(tǐ),其中(zhōng)包含兩個基因,并使用(yòng)IRES或2A等元件用(yòng)一個啓動子共表達它們。如果滴度很(hěn)高,不同rAAV的共轉染率也相當高。所以如果不能(néng)将兩個基因同時放在一個載體(tǐ)中(zhōng),您可(kě)以考慮共轉染方式(盡管這可(kě)能(néng)并不總是在體(tǐ)内有(yǒu)效)。
2、特異性:有(yǒu)一些不同的rAAV成分(fēn)可(kě)以驅動特定細胞/組織中(zhōng)的基因表達; 這些成分(fēn)包括啓動子,Flp或Cre依賴性基因開關,以及血清型(血清型将在下面更詳細地讨論)。如果您的目标是廣泛表達,那麽廣泛活躍的啓動子,如CAG(具(jù)有(yǒu)CMV即時早期增強子的雞β肌動蛋白啓動子),是一個不錯的選擇。如果您有(yǒu)特定的靶細胞類型,您可(kě)能(néng)想嘗試不同的啓動子,例如,CamkIIa具(jù)有(yǒu)神經元特異性。另一方面,具(jù)有(yǒu)Cre或Flp依賴性基因表達的rAAV載體(tǐ)可(kě)以注射到具(jù)有(yǒu)在特定細胞類型中(zhōng)表達Cre或Flp的動物(wù)中(zhōng),導緻僅在這些細胞中(zhōng)進行基因表達。
3、血清型:衣殼蛋白是rAAV載體(tǐ)非常重要的組分(fēn),它可(kě)以驅動這些載體(tǐ)的生物(wù)學(xué)功能(néng)。雖然多(duō)項研究表明不同的血清型在感染不同類型細胞的能(néng)力方面存在差異,但最近的一項研究表明,大多(duō)數(或所有(yǒu))血清型使用(yòng)相同的受體(tǐ)(AAVR)(Pillay et al., 2016)。觀察到的這種趨向性可(kě)能(néng)是由于其他(tā)因素,例如病毒體(tǐ)附着到細胞表面,或者可(kě)能(néng)是進入後的步驟,例如:脫殼。
AAV術語可(kě)能(néng)令人困惑。您可(kě)能(néng)會看到AAV2/2或AAV2/8等名(míng)稱,但這些數字實際上意味着什麽?第一個數字代表反向末端重複(ITR)類型。ITRs是AAV基因組側端的短DNA序列,允許其在宿主細胞中(zhōng)形成多(duō)聯體(tǐ)。它們與Rep蛋白一起促進基因與人類基因組在第19号染色體(tǐ)上AAVS1位點的整合,這種情況隻能(néng)在野生型AAV中(zhōng)觀察到 - 而不是載體(tǐ)形式。幾乎所有(yǒu)載體(tǐ)都含有(yǒu)2型ITR。2型ITR可(kě)以與各種衣殼類型一起包裝(zhuāng)。用(yòng)于包裝(zhuāng)rAAV載體(tǐ)的衣殼類型,即血清型-由第二個數字表示。例如,如果rAAV載體(tǐ)具(jù)有(yǒu)類型2的ITR和類型8的衣殼,則其将表示為(wèi)AAV2/8。
4、基因組:野生型AAV是單鏈DNA病毒。在脫殼DNA後,病毒依賴宿主細胞複制機制來合成互補DNA鏈。該步驟被認為(wèi)是rAAV的轉導效率的限制因素。為(wèi)了克服這個問題,科(kē)學(xué)家(McCarty et al)通過改變一種ITRs來合成二聚體(tǐ)或自身互補的AAV(稱為(wèi)scAAV)。scAAV載體(tǐ)比ssAAV能(néng)更快速起效(幾天)且具(jù)有(yǒu)更高水平的轉基因表達。然而,它們的基因載量(<2.5Kb)是ssAAV(<4.8Kb)的一半,這限制了可(kě)成功包裝(zhuāng)的基因和調控元件的數量。
如果您需要快速轉基因表達,scAAV可(kě)能(néng)很(hěn)适用(yòng)。較低的滴度就可(kě)能(néng)達到所需的轉基因表達水平,從而減小(xiǎo)由于高病毒濃度帶來的毒性或免疫原性。
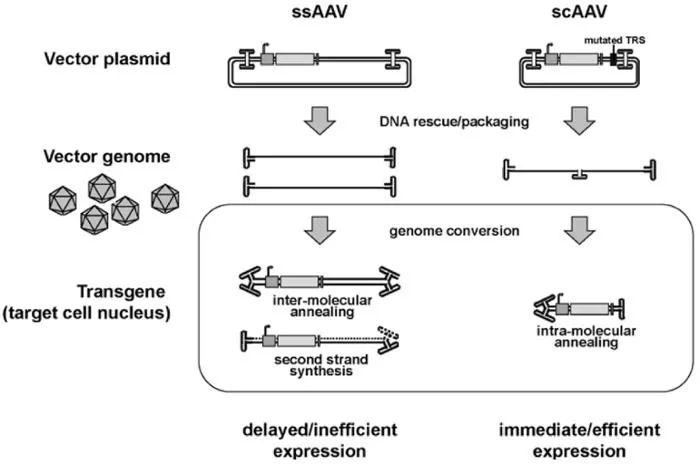
Figure 1: Comparison of ssAAV and scAAV genomes, packaging, and transduction. From Takashi Okada (2013). Efficient AAV Vector Production System: Towards Gene Therapy for Duchenne Muscular Dystrophy, Gene Therapy - Tools and Potential Applications, Dr. Francisco Martin (Ed.), InTech, DOI:10.5772/53023
生産(chǎn)你的rAAV
全世界有(yǒu)幾個公(gōng)司,您可(kě)以從這些地方獲得優質(zhì),高滴度的rAAV(包括Addgene!),當然您也可(kě)以使用(yòng)标準的分(fēn)子生物(wù)學(xué)方法和組織培養經驗在您自己的實驗室中(zhōng)生成rAAV。
簡而言之,您首先用(yòng)攜帶目的基因的rAAV載體(tǐ),腺病毒輔助質(zhì)粒和含有(yǒu)Rep和Cap的質(zhì)粒共轉染HEK293T細胞(圖2,通常稱為(wèi)“三重質(zhì)粒轉染”)。2-3天後,收集上清液(或在某些情況下需要制備細胞提取物(wù),因為(wèi)一些rAAV血清型被釋放到培養基中(zhōng),而其他(tā)類型則沒有(yǒu))(Vandenberghe et al),使用(yòng)PEG從中(zhōng)沉澱病毒粒子。然後使用(yòng)高速的超速離心機通過密度梯度離心進一步純化病毒顆粒。由于其密度很(hěn)高,病毒粒子會在分(fēn)離液中(zhōng)形成一條帶,你可(kě)以收集這條帶。然後通過透析/緩沖液交換去除密度梯度離心液,并且如果需要可(kě)以進一步濃縮病毒粒子。
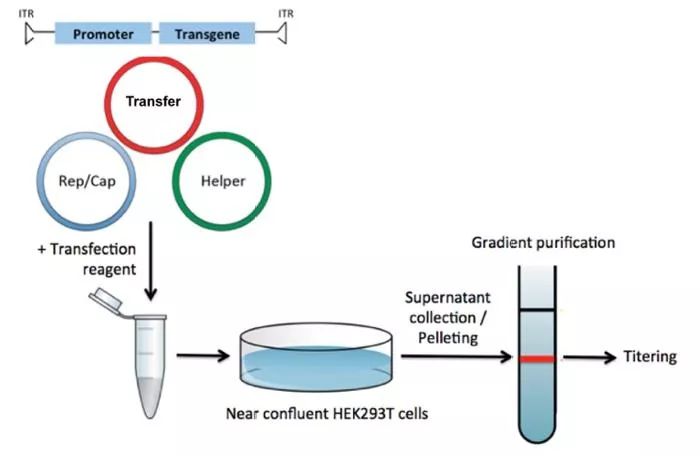
Figure 2: Recombinant AAV (rAAV) transfer vectors typically carry a transgene driven by a promoter of choice between ITRs, but do not encode Rep/Cap. Rep/Cap ORFs encode proteins essential for viral genome replication, virion assembly, and the 60 mer viral capsid. In this case, Rep/Cap are encoded by plasmids that are co-transfected with the transgene plasmid in tissue culture. Also needed for replication is an adenoviral helper plasmid, which induces the lytic life cycle for the AAV, and its release.
體(tǐ)内遞送rAAV
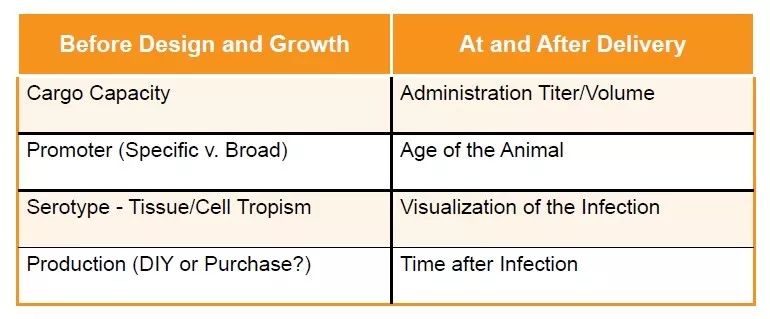
關于AAV在體(tǐ)内的傳遞,有(yǒu)幾個因素是不同的,這取決于您選擇的生物(wù)系統。這些因素對感染的成功程度有(yǒu)很(hěn)大的影響。無論您的應用(yòng)是什麽,下面列出的一些參數,您可(kě)能(néng)需要在注射病毒之前考慮:
1、注射滴度:到達組織的病毒顆粒的數量,将取決于您的病毒制備的滴度和可(kě)以遞送的最大體(tǐ)積,并且這些非常重要。不幸的是,如上所述,病毒的滴度不能(néng)直接轉化為(wèi)您在體(tǐ)内觀察到的現象,盡管它是一個起點。您可(kě)以首先搜索文(wén)獻以獲取有(yǒu)關病毒在特定組織中(zhōng)的建議,但通常需要通過嘗試一系列稀釋濃度來确定在體(tǐ)内的最佳劑量。
2、動物(wù)的年齡:首先,重要的是要記住末期分(fēn)化細胞(即有(yǒu)絲分(fēn)裂後期細胞)将具(jù)有(yǒu)長(cháng)期AAV表達能(néng)力,但是在分(fēn)裂細胞中(zhōng),表達能(néng)力将會喪失。待注射動物(wù)的年齡将确定您可(kě)以成功感染的細胞類型(即在早期發育時間點,尚未出生的細胞,即使其有(yǒu)絲分(fēn)裂祖細胞存在,也不能(néng)被AAV感染)(Xiong and Cepko)。
3、感染的可(kě)視化:在開始感染過程之前,您還應該考慮如何可(kě)視化您的rAAV感染。您是否在rAAV構建體(tǐ)中(zhōng)包含了報告基因,例如GFP或mCherry?能(néng)夠通過熒光測量直接觀察到病毒表達發生的位置。如果沒有(yǒu),您可(kě)以考慮在驅動您感興趣的基因的同一啓動子下共同注射攜帶報告基因的AAV,并測量報告基因表達作(zuò)為(wèi)您感興趣的不易檢測基因的代表。如果無法進行共表達或共感染,通過免疫組化或原位雜交檢測目的蛋白可(kě)能(néng)是您最好的選擇。
4、感染後的時間:注射和組織處理(lǐ)之間需要适當的時間來檢測AAV介導的基因表達。時間将高度取決于衣殼類型和您感染的組織。等待~2周是許多(duō)組織的較好選擇。據報道,AAV介導的基因表達非常穩定,在人類臨床試驗和狗中(zhōng)持續數年(Wonjo et al)。
AAV是用(yòng)于病毒基因傳遞的極其通用(yòng)的工(gōng)具(jù)。您特定研究應用(yòng)的要求将決定AAV設計和遞送的參數。雖然您的最終血清型/滴度/年齡測定将嚴重依賴于預實驗,但您可(kě)以查看越來越多(duō)的文(wén)獻,了解不同生物(wù)系統的設計建議方案。在過去的二十年中(zhōng),有(yǒu)超過一百個涉及AAV的臨床試驗,這個工(gōng)具(jù)似乎在未來幾年仍是治療和基礎研究環境中(zhōng)的熱點。
【參考文(wén)獻】
1. Atchison, Robert W., Bruce C. Casto, and William McD Hammon. “Adenovirus-associated defective virus particles.” Science 149.3685 (1965): 754-755. PubMed PMID: 14325163.
2. Pillay, S., et al. “An essential receptor for adeno-associated virus infection.” Nature 4:520(7588):108-12 (2016). PubMed PMID: 26814968.
3. McCarty, D. M., Paul E. Monahan, and Richard J. Samulski. “Self-complementary recombinant adenoassociated virus (scAAV) vectors promote efficient transduction independently of DNA synthesis.” Gene therapy 8.16 (2001). PubMed PMID: 11509958.
4. Vandenberghe, Luk H., et al. “Efficient serotype-dependent release of functional vector into the culture medium during adeno-associated virus manufacturing.” Human gene therapy 21.10 (2010): 1251-1257. PubMed PMID: 20649475. PubMed Central PMCID: PMC2957237.
5. Veldwijk, Marlon R., et al. “Development and optimization of a real-time quantitative PCR-based method for the titration of AAV-2 vector stocks.”Molecular Therapy 6.2 (2002): 272. PubMed PMID: 12349826.
6. Xiong, Wenjun, and Constance Cepko. “Distinct expression patterns of AAV8 vectors with broadly active promoters from subretinal injections of neonatal mouse eyes at two different ages.” Retinal Degenerative Diseases. Springer International Publishing, 2016. 501-507. PubMed PMID: 26427452.
7. Okada, Takashi. Efficient AAV Vector Production System: Towards Gene Therapy For Duchenne Muscular Dystrophy. INTECH Open Access Publisher, 2013. Intech Webpage.
8. Wojno, Adam P., Eric A. Pierce, and Jean Bennett. “Seeing the light.” Science translational medicine 5.175 (2013): 175fs8-175fs8. PubMed PMID: 23467559.
以上内容來源于Addgene。
 京公(gōng)網安(ān)備11010502040370号 技(jì )術支持:青雲軟件
京公(gōng)網安(ān)備11010502040370号 技(jì )術支持:青雲軟件