文(wén)獻分(fēn)享 | 器官芯片助力肺模型構建和環境毒理(lǐ)學(xué)研究

研究背景
摘要
納米塑料在空氣中(zhōng)普遍存在,容易被吸入,對呼吸健康構成威脅。然而,關于納米塑料對肺損傷特别是慢性阻塞性肺疾病(COPD)影響的研究卻寥寥無幾。此外,細胞和動物(wù)模型無法深入理(lǐ)解由污染物(wù)引發的COPD。現有(yǒu)的肺芯片模型也缺乏與免疫細胞間的相互作(zuò)用(yòng),這對于監測複雜的反應至關重要。本研究構建了一種肺芯片,能(néng)夠準确再現肺泡-微血管屏障的結構特征和關鍵功能(néng),并整合了多(duō)種免疫細胞。通過多(duō)種環境污染物(wù)的毒理(lǐ)學(xué)應用(yòng),展示了肺芯片模型的穩定性和可(kě)靠性。研究進一步探索了COPD與聚苯乙烯納米塑料(PS-NPs)的相關性。結果顯示,随着PS-NPs濃度的增加,細胞活性顯著降低,同時跨膜電(diàn)阻(Teer)水平降低,滲透性增加。此外,PS-NPs能(néng)在器官層面上誘導氧化應激和炎症反應,并穿越肺泡-微血管屏障進入血液循環。α1-抗胰蛋白酶(AAT)的表達顯著降低,可(kě)以作(zuò)為(wèi)早期COPD檢查點。總的來說,肺芯片為(wèi)研究納米塑料的肺毒性提供了一個新(xīn)平台,證明PS-NPs能(néng)損害肺泡-微血管屏障,造成氧化損傷和炎症,增加COPD的風險。
研究内容
肺泡模型構建和驗證
首先将培養好的人肺泡上皮細胞(HPAEpiC)接種到芯片的上腔室,之後将芯片倒置在下層腔室接種人臍靜脈血管内皮細胞(HUVEC),培養一段時間後,利用(yòng)流體(tǐ)控制系統在上腔室注入空氣取代上腔室中(zhōng)的培養基,在下腔室連續灌注培養基,以建立氣體(tǐ)-液體(tǐ)界面(ALI)培養環境,培養若幹天後,将巨噬細胞接種到HPAEpiC細胞表面,之後再動态培養24-48小(xiǎo)時,構建好的肺芯片模型能(néng)夠模拟體(tǐ)内的肺泡-毛細血管屏障結構(圖1,圖2A)。
在肺芯片中(zhōng),光學(xué)成像和基于熒光的活/死細胞染色成像顯示上下腔室的上皮細胞和内皮細胞均形成了連續的細胞層(圖2B和C)。基于熒光共聚焦成像的三維重構也表明培養室中(zhōng)的細胞趨向于逐漸形成連續層,從而構建出完整的上皮和内皮層(圖2D)。緊密連接蛋白(E-鈣粘蛋白和VE-鈣粘蛋白)的陽性表達以及氣液培養過程中(zhōng)穩定的跨膜電(diàn)阻(Teer)值均表明在芯片上構建了結構完整和生理(lǐ)功能(néng)完善的肺泡-毛細血管屏障(圖2E和F)。同時肺芯片能(néng)夠維持穩定超過兩周。
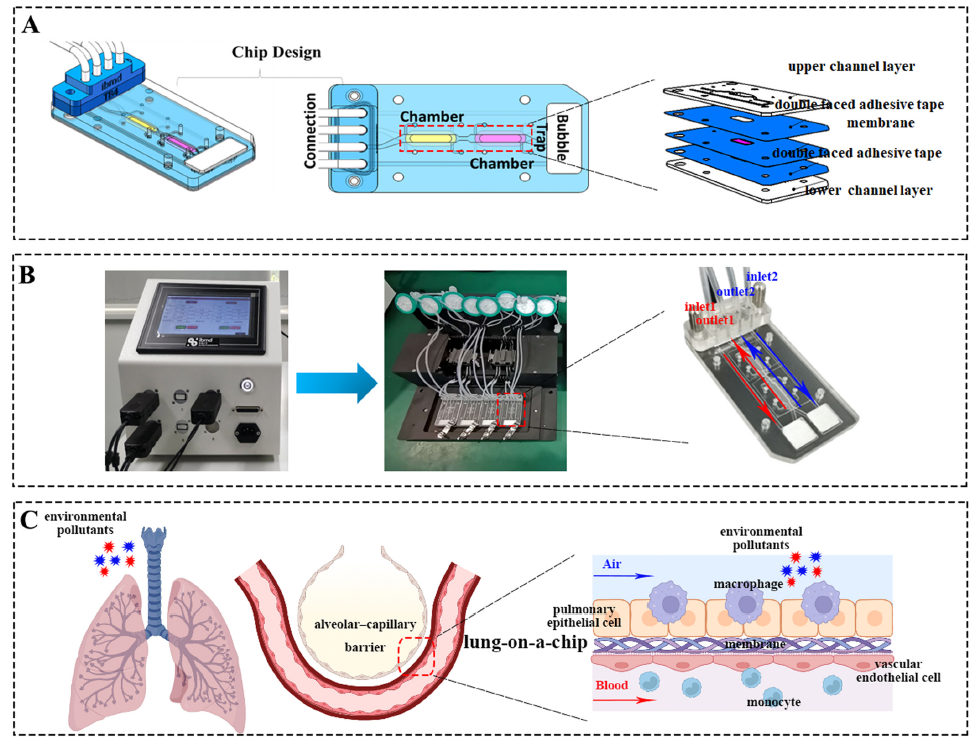
圖 1. 肺芯片系統。A:肺芯片設計和加工(gōng);B:流體(tǐ)控制系統;C:肺芯片和PS-NPs暴露示意圖。
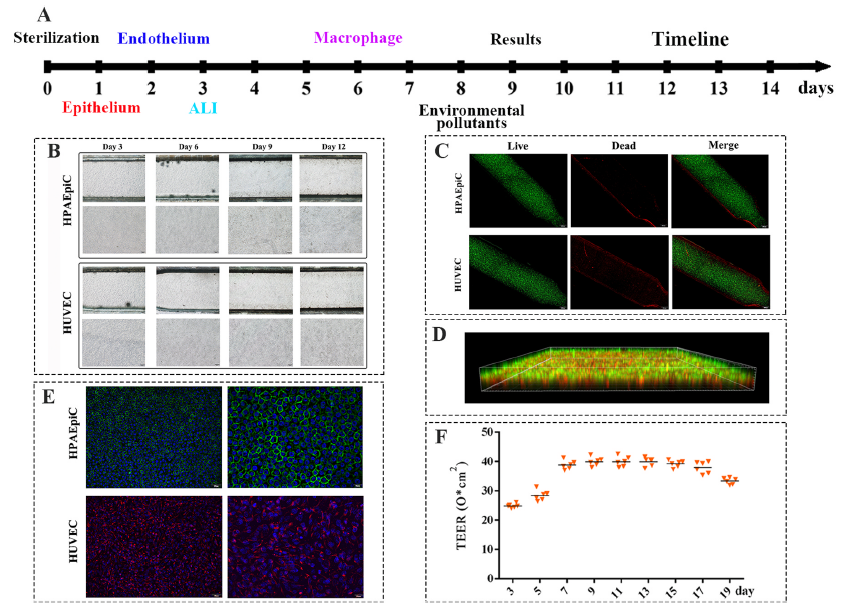
圖2 肺模型構建和特征。A: 肺芯片構建時間線(xiàn);B: 肺芯片明場成像;C: 死活細胞染色;D: 肺芯片熒光共聚焦成像3D重構圖;E: 緊密連接蛋白免疫熒光;F:氣液培養過程中(zhōng)肺模型TEER值變化。
肺芯片可(kě)以作(zuò)為(wèi)環境毒理(lǐ)學(xué)研究平台
通過測試肺芯片暴露于不同種類的代表性環境污染物(wù)中(zhōng)的表現,可(kě)以用(yòng)于建立環境毒理(lǐ)學(xué)研究平台。本研究将構建的肺芯片模型暴露于不同種類(生物(wù)氣溶膠、化學(xué)污染物(wù)和納米顆粒)的環境污染物(wù)(脂多(duō)糖、銅納米顆粒、銀納米顆粒、氧化鋅納米顆粒、氧化鋁納米顆粒、香煙煙霧提取物(wù))24h,通過死活細胞染色成像和細胞活性分(fēn)析顯示,在熒光圖像中(zhōng)芯片中(zhōng)的活細胞數量顯著減少,而死細胞數量增加(圖3A),同時細胞活性顯著降低(圖3B)。同時通過檢測TEER值和滲透系數值以及熒光标記的葡聚糖定量,結果均表明環境污染物(wù)破壞了模型的屏障功能(néng)(圖3C&3D)。進一步通過分(fēn)析肺損傷相關的炎症因子分(fēn)泌、活性氧(ROS)生成、THP-1(人白血病單核細胞)細胞粘附、抗胰蛋白酶(AAT,COPD标志(zhì)物(wù))表達(圖4),顯示肺芯片可(kě)以從多(duō)個維度分(fēn)析環境污染物(wù)對于呼吸系統健康的損害,如炎症因子釋放、更多(duō)的單核細胞粘附血管内皮細胞層、ROS過量生成、AAT表達減少,證明作(zuò)為(wèi)一種穩定和可(kě)靠的模型,肺芯片系統可(kě)以用(yòng)于不同環境污染物(wù)的毒理(lǐ)學(xué)研究。
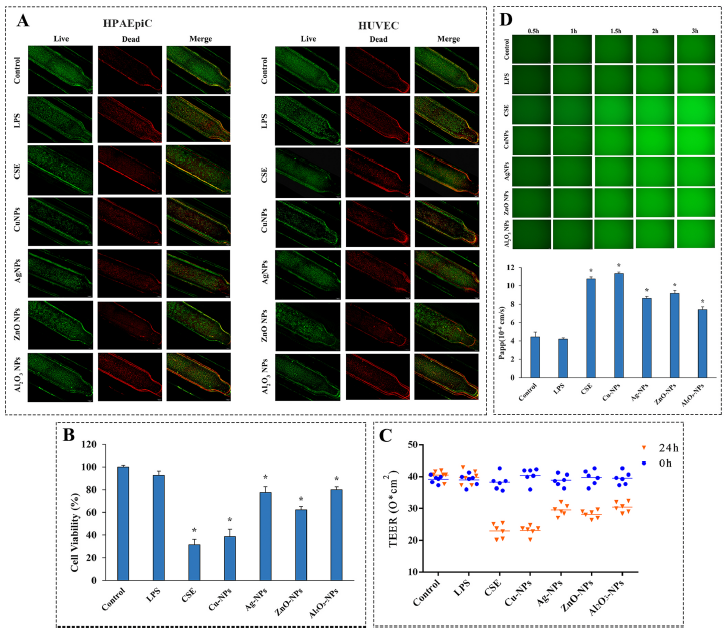
圖3 肺芯片環境污染物(wù)毒理(lǐ)學(xué)應用(yòng)。A: 環境污染物(wù)暴露後死活細胞染色;B: 不同環境污染物(wù)的細胞活性;C: TEER值;D: 熒光标記小(xiǎo)分(fēn)子從肺泡腔轉移到血管腔的延時成像和滲透系數值。
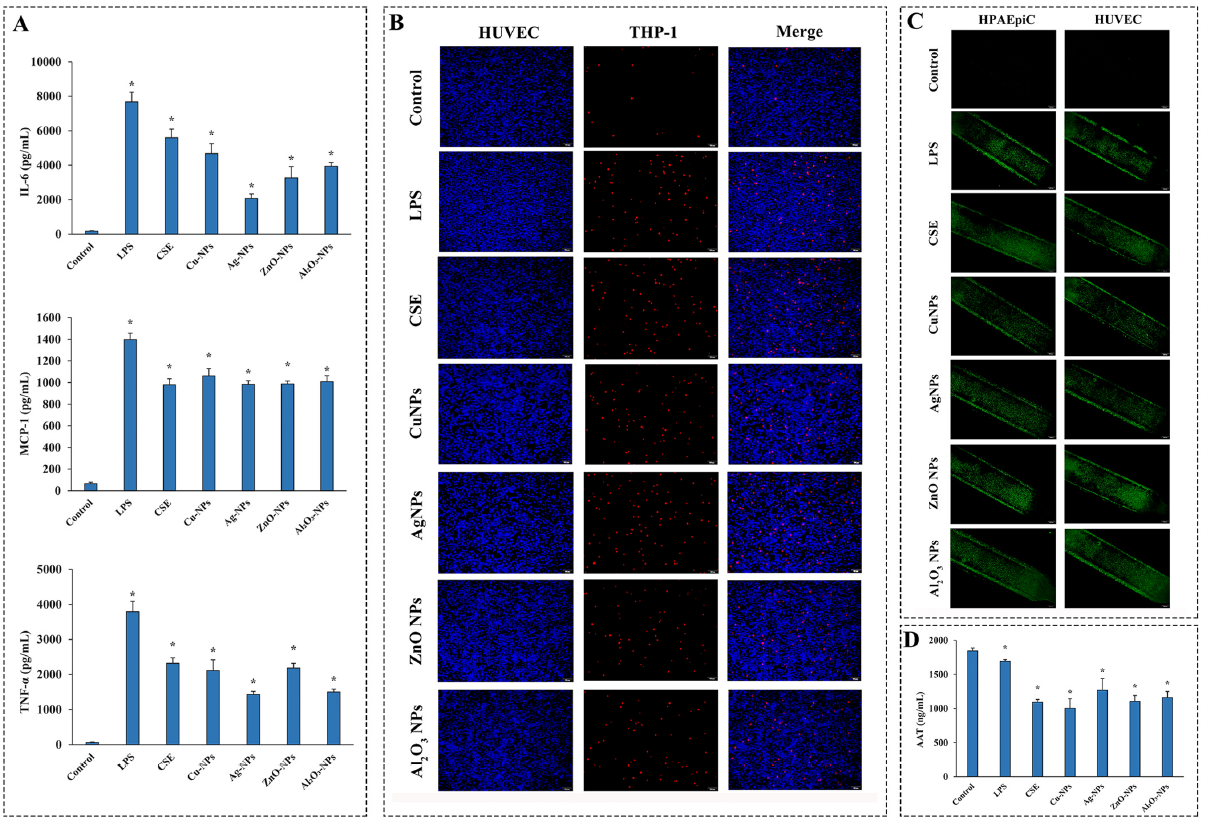
圖4 肺芯片用(yòng)于環境污染物(wù)毒理(lǐ)學(xué)研究。A: IL-6, MCP-1和TNF-α表達(ELISA方法);B: THP-1細胞粘附(熒光成像);C: 活性氧(ROS)生成(熒光成像);D: 抗胰蛋白酶(AAT)表達(ELISA方法)。
利用(yòng)肺芯片探索聚苯乙烯納米塑料(PS-NPs)與COPD的相關性
在模型暴露于PS-NPs 24小(xiǎo)時後,通過死活細胞雙熒光染色分(fēn)析,結果表明納米塑料以劑量效應的方式引起人肺上皮細胞和人臍靜脈内皮細胞的死亡(圖5A),其中(zhōng)低劑量和中(zhōng)等劑量的PS-NPs(7.5和15μg/cm²)對細胞活力基本無影響,但30μg/cm²的PS-NPs顯著抑制了細胞活力(圖5B)。結合低劑量下TEER值增加,猜測這可(kě)能(néng)由于保護性應激反應。綜合分(fēn)析不同劑量下的TEER值和FITC-葡聚糖擴散,結果均表明PS-NPs能(néng)破壞肺泡-毛細血管屏障的結構完整性和屏障功能(néng)(圖5C&5D)。
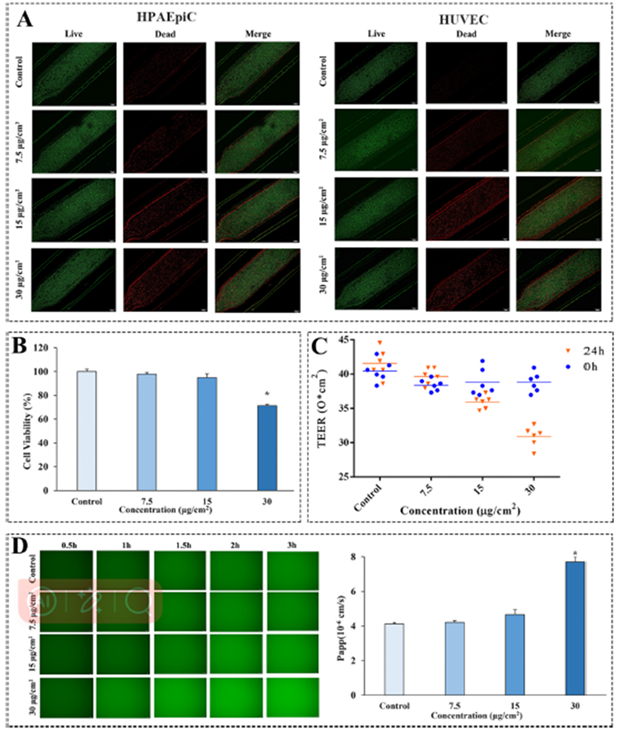
圖5 PS-NPs破壞肺泡-毛細血管屏障。A: PS-NPs 暴露後死活細胞染色;B: 細胞活性分(fēn)析;C: PS-NPs暴露前後TEER變化;D: 不同PS-NPs濃度下的滲透系數。
将單核細胞灌注到血管通道以研究肺芯片在PS-NPs刺激下引發的炎症介導的免疫反應,結果顯示細胞因子(IL-6、MCP-1和TNF-α)的水平在不同劑量暴露下均呈現顯著增長(cháng)(圖6A)。同樣,在不同劑量組中(zhōng)均觀察到大量的THP-1細胞粘附在内皮層上(圖6B),表明在肺芯片中(zhōng)不同細胞之間存在相關交流。作(zuò)為(wèi)炎症進展中(zhōng)的重要信号分(fēn)子,研究人員進一步檢測了活性氧(ROS)的生成,由PS-NPs誘導ROS生成表現出劑量-效應關系。有(yǒu)趣的是,在較低劑量暴露下HUVEC細胞的熒光信号比HPAEpiC顯著更弱,而在高劑量下兩種細胞的ROS生成相當,這也證實了模型的屏障功能(néng)及細胞間存在相互作(zuò)用(yòng)。(圖6C)。
為(wèi)了評估PS-NPs與細胞的相互作(zuò)用(yòng),研究人員通過流式細胞術測量了肺芯片中(zhōng)PS-NPs的攝取情況。實驗結果顯示,PS-NPs以劑量依賴的方式在人肺上皮細胞/巨噬細胞、人臍靜脈内皮細胞和THP-1細胞中(zhōng)積累。其中(zhōng),PS-NPs在上皮細胞的内化率遠(yuǎn)高于其他(tā)細胞類型,僅在高劑量下觀察到THP-1細胞對PS-NPs的攝取量增加(圖6D)。結果同時還表明,PS-NPs首先被人肺上皮細胞/巨噬細胞攝取,通過破壞肺泡-毛細血管屏障,随後進入血液系統影響其他(tā)器官。為(wèi)了進一步确認PS-NPs對慢性阻塞性肺疾病(COPD)風險的影響,研究人員檢測了抗胰蛋白酶(AAT)的表達。在芯片經PS-NPs處理(lǐ)後,觀察到了AAT值以劑量依賴性方式顯著降低(圖6E)。
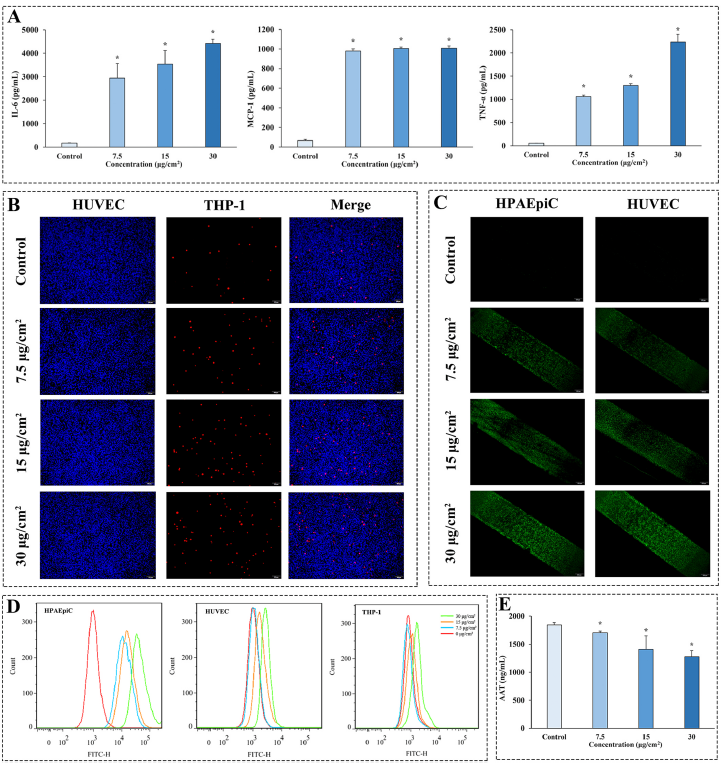
圖6 PS-NPs暴露下肺芯片的反應。A: IL-6, MCP-1和TNF-α表達情況;B: THP-1細胞粘附情況;C: PS-NPs 暴露後ROS的生成;D: 肺芯片中(zhōng)PS-NPs 的攝取和轉運;E: AAT表達情況
結論
本研究利用(yòng)膜式芯片和流控系統構建了一種肺芯片模型,旨在重現肺泡-毛細血管屏障的關鍵結構,通過引入免疫系統可(kě)以更真實地模拟體(tǐ)内的微環境,提高了免疫反應的效果和敏感性。通過在該肺芯片系統直觀的監測不同種類環境污染物(wù)引起的肺損傷,包括屏障功能(néng)障礙、氧化損傷和炎症反應,展示了肺芯片在環境毒理(lǐ)學(xué)研究中(zhōng)的應用(yòng)價值。進一步分(fēn)析PS-NPs暴露後所引起的氧化應激、炎症反應和AAT功能(néng)受損以及肺芯片中(zhōng)PS-NPs的攝取和轉運情況,證實PS-NPs是通過破壞肺泡-毛細血管屏障而進入血液循環,這可(kě)能(néng)會增加發展為(wèi)COPD的風險。
參考文(wén)獻:
Yang S, Zhang T, Ge Y, et al. Sentinel supervised lung-on-a-chip: A new environmental toxicology platform for nanoplastic-induced lung injury. J Hazard Mater. 2023;458:131962
 京公(gōng)網安(ān)備11010502040370号 技(jì )術支持:青雲軟件
京公(gōng)網安(ān)備11010502040370号 技(jì )術支持:青雲軟件